
- English
- 简体中文
- Español
- Português
- русский
- Français
- 日本語
- Deutsch
- tiếng Việt
- Italiano
- Nederlands
- ภาษาไทย
- Polski
- 한국어
- Svenska
- magyar
- Malay
- বাংলা ভাষার
- Dansk
- Suomi
- हिन्दी
- Pilipino
- Türkçe
- Gaeilge
- العربية
- Indonesia
- Norsk
- تمل
- český
- ελληνικά
- український
- Javanese
- فارسی
- தமிழ்
- తెలుగు
- नेपाली
- Burmese
- български
- ລາວ
- Latine
- Қазақша
- Euskal
- Azərbaycan
- Slovenský jazyk
- Македонски
- Lietuvos
- Eesti Keel
- Română
- Slovenski
- मराठी
- Srpski језик
Millised on farmaatsiavahendite kategooriad?
Farmaatsiatööstuse ahelas farmaatsiasvahepealon aktiivsete farmaatsiakoostiste sünteesimise peamised eellased (API -d. Need kajastavad otseselt ravimite teadus- ja arendustegevuse tehnilisi marsruute ja terapeutilise piirkonna jaotust. Need ühendid valmistatakse spetsiifiliste keemiliste reaktsioonide kaudu. Seejärel läbivad nad API -deks selliseid samme nagu kondensatsioon, atsüülimine ja kiraalne süntees. Farmatseutiliste vaheühendite kvaliteet ja pakkumise stabiilsus mõjutavad ravimite tootmise tõhusust. Siin on nende klassifitseerimissüsteemi ja tööstuse rakenduste jaotus neljast peamisest mõõtmest.
Klassifikatsioon terapeutilise piirkonna järgi: sihitud nõudlus täpse positsioneerimise järele
Kasvajavastased vaheühendid on viimastel aastatel kõige kiiremini arenev kategooria. Näiteks nõuab PD-1 inhibiitori vaheühendite süntees mitmeid sidumisreaktsioone, näiteks 2-fluoro-5-klorobensoehapet kui immuunravimite, näiteks kamrelizumabi ettevalmistamise võtmevaheühendit. ALK -sihtmärgi jaoks peab brigatiniibi vaheühend konstrueerima bifenüülistruktuuri Suzuki sidumisreaktsiooni kaudu, puhtusevajadusega üle 99,5%.
Antimikroobsed vaheühendid katavad antibiootikumid, viirusevastased ja muud väljad. Näiteks 7-aminotsephalosporanhape (7-ACA), kui tsefalosporiini ravimite tuumvaheühend, saadakse tsefalosporiin C lõhustumise kaudu; HIV -ravimi vahepealse ritonaviiri kiraalne amiini struktuur nõuab ettevalmistamiseks ensümaatilise eraldusvõime tehnoloogia kasutamist.
Kardiovaskulaarseid vaheühendeid esindavad statiiniravimite vaheühendid, näiteks atorvastatiini vaheühend (3R, 5R) -dihüdroksü heptaanhappe laktoon, mis nõuab asümmeetrilist hüdrogeenimisreaktsiooni, et ehitada korpuse keskus, mille optiline puhtus on üle 99%, nt.
Klassifikatsioon keemiliste struktuuriliste omaduste järgi: molekulaarsete luustikke teaduslik jagunemine
Heterotsüklilised vaheühendid moodustavad pooled farmaatsiavaheühenditest, kõige tavalisemad on lämmastikku sisaldavad heterotsüklid. Näiteks kasutatakse pürrolopüridiini vaheühendeid JAK inhibiitorite, piperasiini vaheühendite (näiteks 1-tert-butoksükarbonüül-piperasiini) sünteesis on psühhotroopsetes ravimites tavalised struktuuriühikud ja puriini vaheühendid kasutatakse laialdaselt vastu antiviraalseid ravimeid nagu antikycloviir).
Kiraalsetel vaheühenditel on stereokeemia kontrolli tõttu kõrged tehnilised tõkked. Näiteks tuleb talidomiidi (S) -konfiguratsiooni vaheühend olla ette valmistatud kiraalse allika sünteesi või kineetilise eraldusvõime kaudu ning selle optiline puhtus mõjutab otseselt ravimite ohutust. Viimastel aastatel on pideva voolu kiraalse katalüüsi tehnoloogia rakendamine vähendanud selliste vahendite tootmiskulusid enam kui 30%.
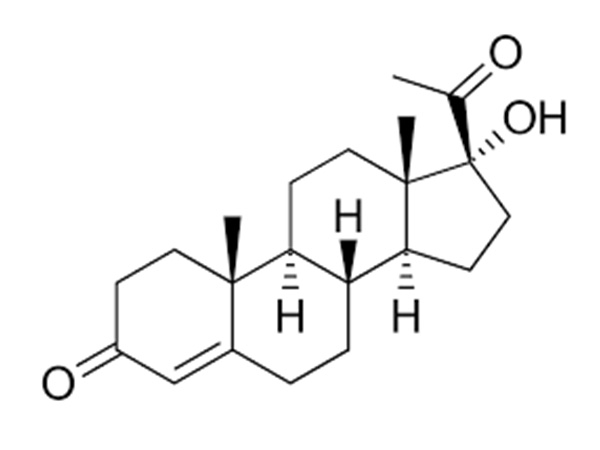
Steroidsed vaheühendid saadakse looduslike steroidsete ühendite modifitseerimisel, näiteks diosgeniinist valmistatud prednisolooni vaheühend, mis nõuab mitmeid reaktsioone, näiteks oksüdatsioon ja hüdrolüüs. Sünteesi võti on steroidse tuuma konfiguratsiooni säilitamine.
Klassifikatsioon sünteesi etapi ja väärtuse järgi: tööstusahela hierarhia selge määratlus
Algvaheühendid on enamasti saadud põhilistest keemilistest toorainetest, näiteks aniliini nitreerimisel saadud p-nitroaniliinist, mida kasutatakse sulfoonamiidravimite lähtematerjalina ja millel on rikkalik turupakkumine, kus on väikeste hinna kõikumistega.
Peamised vaheühendid viitavad sünteesi marsruudi põhisammudele, mis määravad ravimi aktiivse rühma moodustumise. Näiteks nõuab Oseltamiviri peamine ühekordse tsüklopentenekarboksüülhapet kuuearvestatud tsükli struktuuri ehitamist läbi Diels-Alderi reaktsiooni, millel on kõrge sünteesi keerukus ja ühe kilogrammi hind, mis võib olla 5-10-kordne tavalistest stardivahenditest.
Kohandatud vaheained on kohandatud innovaatiliste ravimite uurimiseks ja arendamiseks. Näiteks peab teatud ADC ravimi linkeri vaheühend vastama sellistele omadustele nagu resistentsus ensümaatilise hüdrolüüsi ja lõhustavuse suhtes, kasutades sageli spetsiaalseid protsesse, näiteks tahkefaasi süntees või fluorini modifikatsioon. Tootmisskaala algab tavaliselt grammi tasemel ning teadus- ja arendustsükkel võib kesta 12–18 kuud.
Klassifikatsioon tootmistehnoloogia teel: suunamisjuhised protsessiinnovatsiooni jaoks
Keemiliste sünteesi vaheühendid jäävad peavooluks. Näiteks kasutatakse süsinik-süsinikusidemete ehitamiseks GRIgnardi reaktiivide vaheühendeid; Elektrokeemilise sünteesi tehnoloogia rakendamine on vähendanud nitrobenseeni redutseerimise energiatarbimist, et valmistada aniliinvahendeid 20%. Biokatalüütilistel vaheühenditel on kiraalse sünteesi olulised eelised. Näiteks transaminaasi kasutamine sitagliptiini vaheühendite valmistamisel katalüüsimiseks saavutab 100% aatomimajanduse, vähendades orgaaniliste lahustite kasutamist 90% võrreldes keemiliste meetoditega. Rohelised katalüütilised vaheühendid võtavad kasutusele sellised tehnoloogiad nagu pidevad voolureaktsioonid ja lahustivaba süntees. Näiteks sünteesitakse teatud sartani ravimi vaheühend mikrolaineabi abil sünteesi kaudu, lühendades reaktsiooniaega 8 tunnilt traditsioonilise partii meetodil 20 minutini ja vähendades reovee 75%.
Kuna uuenduslike ravimite areng areneb keerukate sihtmärkide poole, farmatseutilinevahepealarenevad kõrgema aktiivsuse ja selektiivsuse poole. Vaheühendite valimisel peavad ettevõtted pöörama tähelepanu ICH Q3A lisandite kontrolli juhistele. Uute tehnoloogiate nagu voolukeemia ja fotokatalüüs rakendamine suunab vaheühendite tootmist "suure tõhususe, rohelise ja intelligentse" poole, pakkudes tugevamat tuge geneeriliste ravimite järjepidevuse hindamiseks ning innovaatiliste ravimite uurimiseks ja arendamiseks.


